Chiba/Engeneering Flagella
From 2007.igem.org
| Line 76: | Line 76: | ||
===[[Chiba/Flagella/Display_Check2|Display Check2: Beads Adsorption]]=== | ===[[Chiba/Flagella/Display_Check2|Display Check2: Beads Adsorption]]=== | ||
[[Image:Beads-Adsorption.gif|frame|left|fig1]]<br clear="all"> | [[Image:Beads-Adsorption.gif|frame|left|fig1]]<br clear="all"> | ||
| - | *pUC19-FliC-His( | + | *pUC19-FliC-His,をKeio⊿FliC株にトランスフォーメーション。培養液をビーズと懸濁させ、大腸菌をBeadsに吸着する。 |
| - | Co2+ | + | 吸着した大腸菌をbufferで溶出し、inculateする。(Negative Control 1:Noplasmid,Negative Control 2:Co2+あるいはNi2+の有り・無し) |
| - | *pUC19-FliC-His | + | →吸着していなかった |
| - | + | *pUC19-FliC-His,をKeio⊿FliC⊿MotB株にトランスフォーメーション。培養液をビーズと懸濁させ、大腸菌をBeadsに吸着する。 | |
| - | + | 吸着した大腸菌をbufferで溶出し、inculateする。(Negative Control 1:Noplasmid,Negative Control 2:Co2+あるいはNi2+の有り・無し) | |
| + | →吸着していた。 | ||
[[Image:Beads-Adsorption_result.gif|frame|left|fig1|320x240px]]<br clear="all"> | [[Image:Beads-Adsorption_result.gif|frame|left|fig1|320x240px]]<br clear="all"> | ||
Revision as of 08:25, 24 October 2007
|
Introduction | Project Design | Engeneering Flagella | Quorum Sensing | Our Goal || Team Members | メンバ連絡簿 |
Our Aim
大腸菌同士を吸着させるため,我々は(細胞の外側に突出しているもののうち)鞭毛に着目した. (図:イメージ)
About flagella
大腸菌は5~10?本/細胞(<chemotaxisの本で要確認)の鞭毛を持つ.鞭毛を回転/逆回転させることにより環境の良い場所へとtaxisする.鞭毛は長さ約10~15μm,半径約23nmの空孔のチューブ状である.(図:菌全体)
鞭毛のフィラメント部はFliCという蛋白質が規則正しく配列した多量体である.(図:鞭毛アップ)
FliCはD0,D1,D2,D3ドメインを持つ.(種類によってはD1,D2,D3の3つのドメインを持つ)D1とD2はformation of the functional flagellar formation(ffff)の為に必要であるが,D3ドメインは必要でなく可変である(図:蛋白質構造&鞭毛断面図)
(Ref)
"Variable" FliC D3 domain
可変なD3ドメインに他の<__aaまでの>アミノ酸を挿入しても鞭毛が合成される[2]. 詳細も書く.
References
- Kuwajima, G. et al.: Nature Biotechnology, 6, 1080-1083 (1988).
- Tanskanen, J. et. al.: Appl. and Env. Microbiol., 4152-4156 (2000)
Parts Assembly
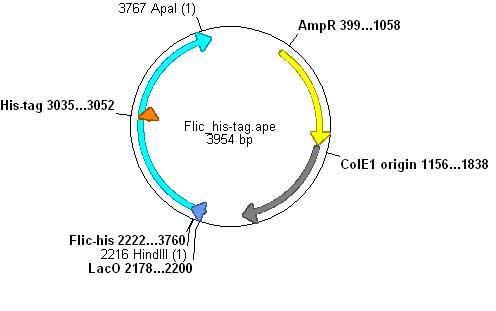
FliC-hisの作成
- FliC遺伝子のD3領域に、Histidineループをコードする遺伝子を挿入し、ヒスチジンタグとして発現させる。
→Linker Ligation
- 完成プラスミド
- Phenotypeをチェック→SDS-PAGE,Western-Blotting
- ヒスチジンタグがFliC遺伝子の外側に発現していることを確認する。
→Beads adsorption
FliC-His generator
- His-tagを入れたFliCをpLuxの下に置き、LuxRが発現されている条件のもとならば、Quorum SensingでFliCを発現させることができるようにする。
- Quorum Sensingのための遺伝子回路がcolEI oriのvectorに乗っているために、p15Aのベクターを使いdouble transformation することでQuorum Sensingと合わせることができるようになる。
- pLuxをもつベクター側とFliCをPCRを使って、Ligationさせることで作る。
FliC-his biobrick
必要なこと
- puc19 vectorの乗っているのでbiobrickのベクターに乗せる。
- 制限酵素サイト(EcoRI,SpeI,PstI)をつぶす。
- FliC His-TagにはEcoRI,SpeI,PstIが含まれているために、そのままではvectorに入れられない。
#片側をblunt end もう一方をApaIの制限酵素サイトをつけ、PCRする。 #vector側も同様にPCRしLigationさせる。
Experiments
Phenotype Check: SDS-PAGE,Western-Blotting
- SDS-PAGE,Western-Blotting
約70kDaにバンドが出ている→FliCが発現していることが確認された
SDS-PAGEを転写。70kDaに抗体抗原反応による茶色いバンドが出た→Histidineの発現が確認された。
Display Check1: Swarming test
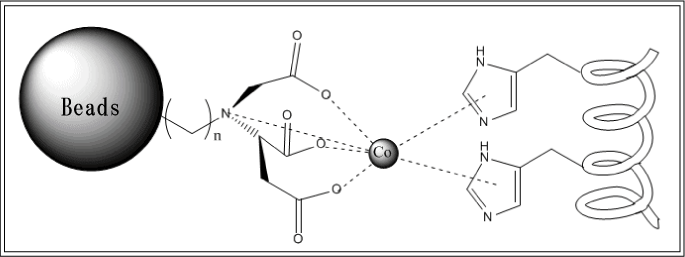
Display Check2: Beads Adsorption
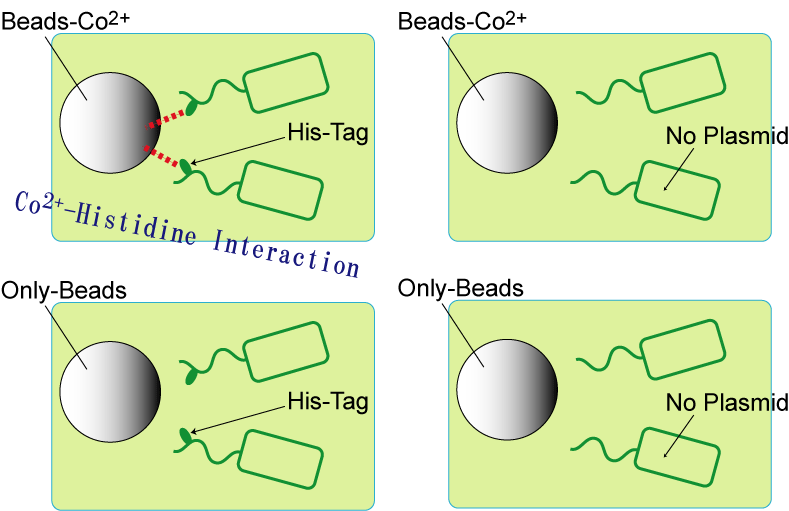
- pUC19-FliC-His,をKeio⊿FliC株にトランスフォーメーション。培養液をビーズと懸濁させ、大腸菌をBeadsに吸着する。
吸着した大腸菌をbufferで溶出し、inculateする。(Negative Control 1:Noplasmid,Negative Control 2:Co2+あるいはNi2+の有り・無し) →吸着していなかった
- pUC19-FliC-His,をKeio⊿FliC⊿MotB株にトランスフォーメーション。培養液をビーズと懸濁させ、大腸菌をBeadsに吸着する。
吸着した大腸菌をbufferで溶出し、inculateする。(Negative Control 1:Noplasmid,Negative Control 2:Co2+あるいはNi2+の有り・無し) →吸着していた。